Stavba - odhlučnění, odvlhčení, reakce na oheň
Sanace zdiva X. – Způsoby snížení vlhkosti zdiva: Elektroosmóza
17. 1. 2023
| Elektroosmotické metody jsou způsoby sanace vytvářející potenciál stejnosměrného elektrického proudu ve zdivu, který potlačuje proces kapilárního vzlínání vody. Jde o metodě přímé sanace vlhkého zdiva určenou pro všechny druhy materiálů a konstrukcí s pórovitou strukturou, ve kterých dochází k pohybu vody působením kapilárních sil. |
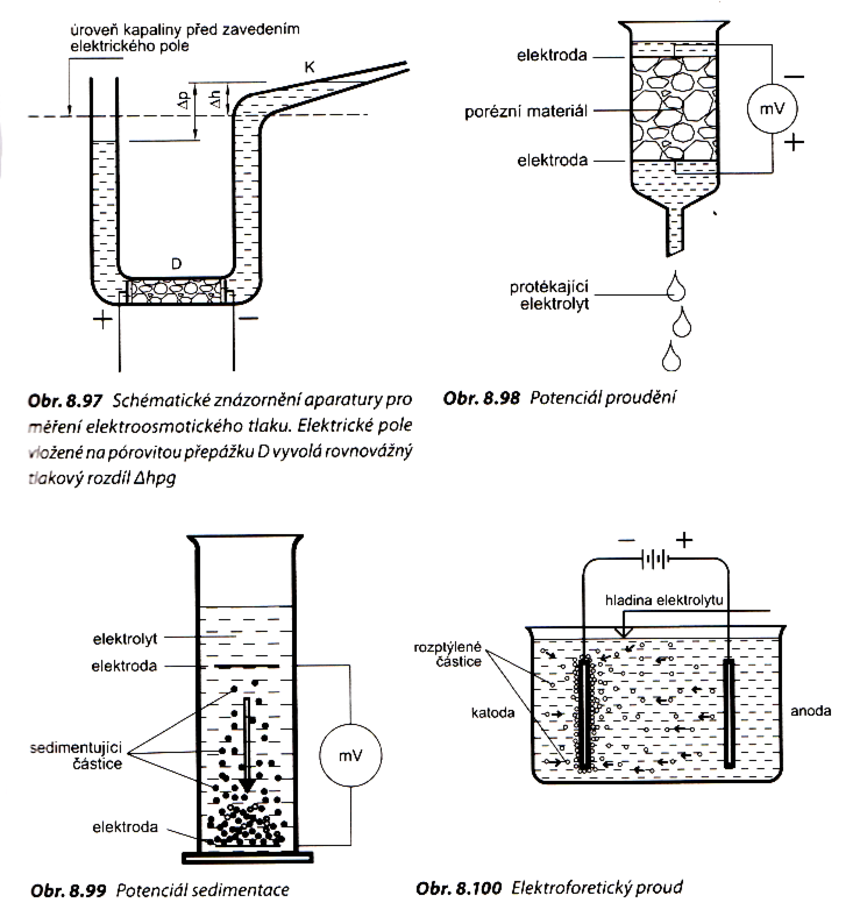
Elektroosmóza
Helmholtz je shrnul do následujících bodů:
Elektrolýza
- vylučování vodíku z molekul vody na katodě;
 |
Zdroj: Odvlhčování staveb Autor: Balík Michael a kolektiv |
-
Nová zelená úsporám: dotace ještě ne, ale teď je čas jednat
› více zde -
19.5. 20.5.Stavební výstava STAVBA - TEPLO - ENERGIE - Veletrh úspor Litomyšl › více zde
-
Nedostatek polystyrenu? Ve skutečnosti jen vlna paniky! › více zde
-
31.3.Webinář Saint-Gobain Fórum: Nová zelená úsporám jinak? Jaká bude jeho budoucnost a pravidla pro rok 2026? › více zde
-
25.3. 28.3.Stavební veletrh BRNO - zdravé bydlení, odborná fóra i řešení pro stavbu a rekonstrukci domů. › více zde
- Zateplení střechy
- Ekologie a energetika
- Zateplování fasády
- Zateplování dřevostaveb
- Názvosloví tepelných izolací
- Izolace a zateplení sklepa
- Pasivní domy
- Stavba - odhlučnění, odvlhčení, reakce na oheň
- Součinitel prostupu tepla
- Tepelné mosty a plísně v domu
- Paropropustnost a difúze
- Třídy reakce na oheň u materiálů
- Objemová hmotnost
- Kondenzace vodní páry
- Tech. postup zateplení fasády
- Návody a typy k zateplení
- Spádování ploché střechy
- Nové hodnoty součinitele prostupu tepla pro budovy(2011)
- Tepelný odpor - výpočty
Skelná vata: Dekwool, Isover, Knauf, Ursa, Ursa PureOne
Minerální vata: Baumit, Isover, Knauf Nobasil, Rockwool
Dřevovláknité desky: Pavatex, Steico, Inthermo, Agepan
Dřevocementové desky: Knauf-Heraklith, DCD Ideal, Velox
EPS - expandovaný polystyren: Baumit, Enroll, Isover, Styrotrade
XPS - extrudovaný polystyren: Austrotherm, Dow Chemical, Isover, Synthos, Ursa
PUR - pěnový polyuretan: Eurothane, ITP, Jitrans Trade, PUR Izolace
PIR izolace: Dekpir, Kingspan, Powerline, PUR Izolace, Pama, Satjam
PE - pěnový polyetylén: Ekoflex, Mirel Trading, Fadopex, Fastrade
Pěnové sklo: Foamglas, Ecotechnics, Recifa
Minerální granuláty: Lias
Materiály na bázi kamenné vlny: Machstav, Knauf, Isover
Materiály na bázi papíru a celulózy: Enroll, CIUR, Dektrade
Sendvičové desky a systémy: Kingspan, Marcegaglia, P-Systems, Ruukki
Ovčí vlna: Naturwool, Isolena, Jiří Faltys
Konopí: Insowool, Canabest, Izolace konopí CZ
Ostatní: Džínovina, OSB desky








